hagamos algunos cálculos usando la ecuación de henderson hasselbeck anteriormente vimos que la ecuación de henderson hazel back es ph es igual a pk a más el logaritmo de la concentración de a menos entre la concentración de h así que estamos hablando de un par conjugado ácido base h y menos ahora para nuestro problema el ácido h sl nh4 más y la base a menos sería nh3 el amoniaco.. Ecuación de Henderson-Hasselbalch. La ecuación de Henderson-Hasselbalch (frecuentemente mal escrito como Henderson-Hasselbach) se utiliza para calcular el pH de una solución buffer o tampón, a partir del pK a (la constante de disociación del ácido) y de las concentraciones de equilibrio del ácido o base, del ácido o la base conjugada.

The HendersonHasselbach equation YouTube

Resolución del ejercicio a través de la ecuación de HendersonHasselbach Química Analítica I
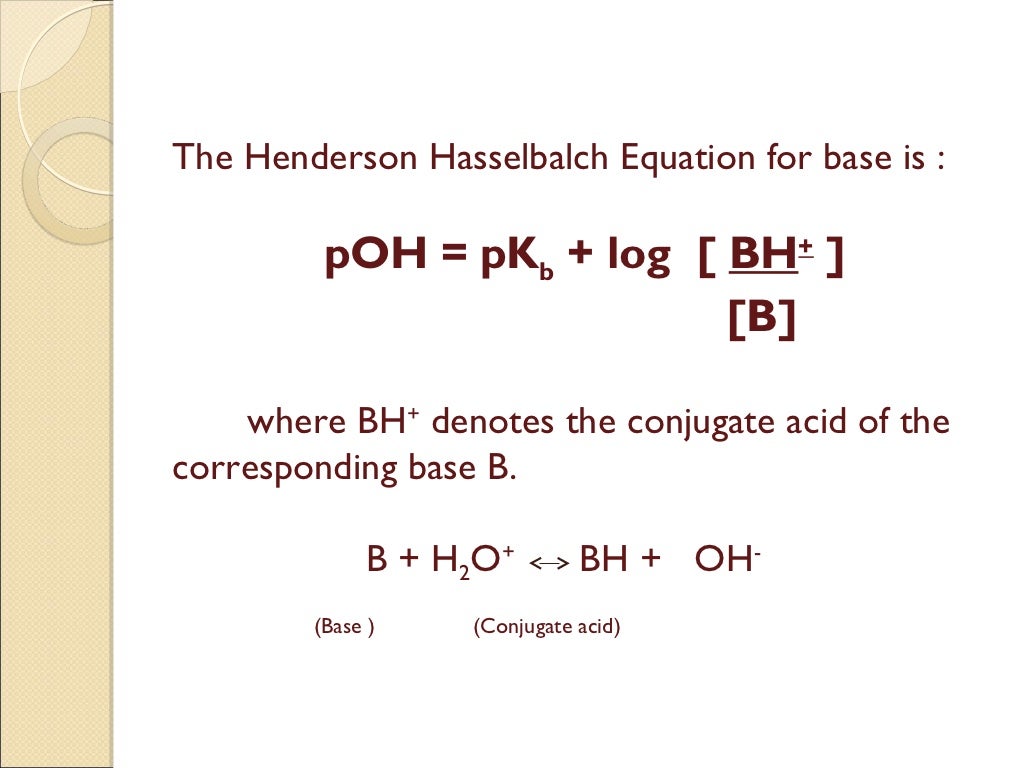
Henderson Hasselbalch Ecuacion
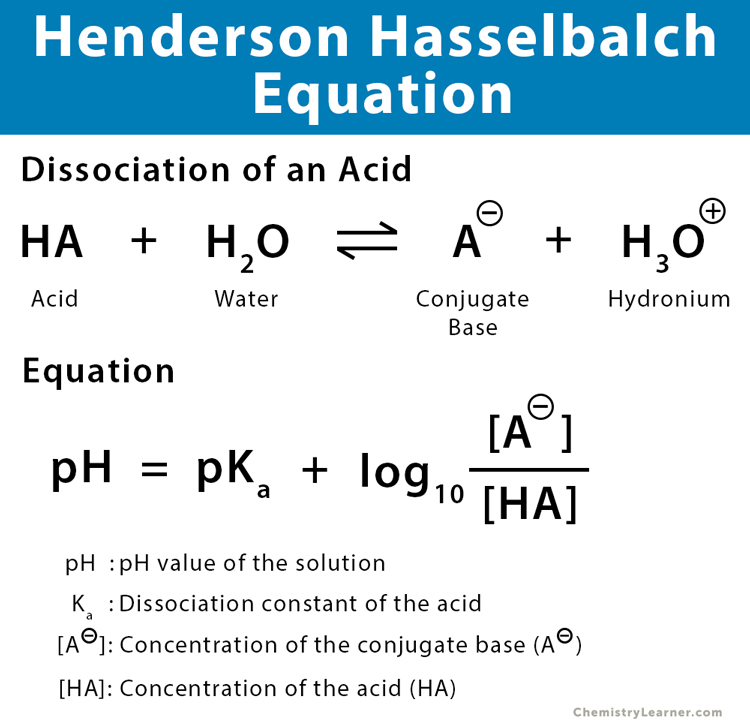
HendersonHasselbalch Equation Derivation and Problems

Henderson Hasselbalch Equation Microbe Notes

Henderson Hasselbalch Ecuacion
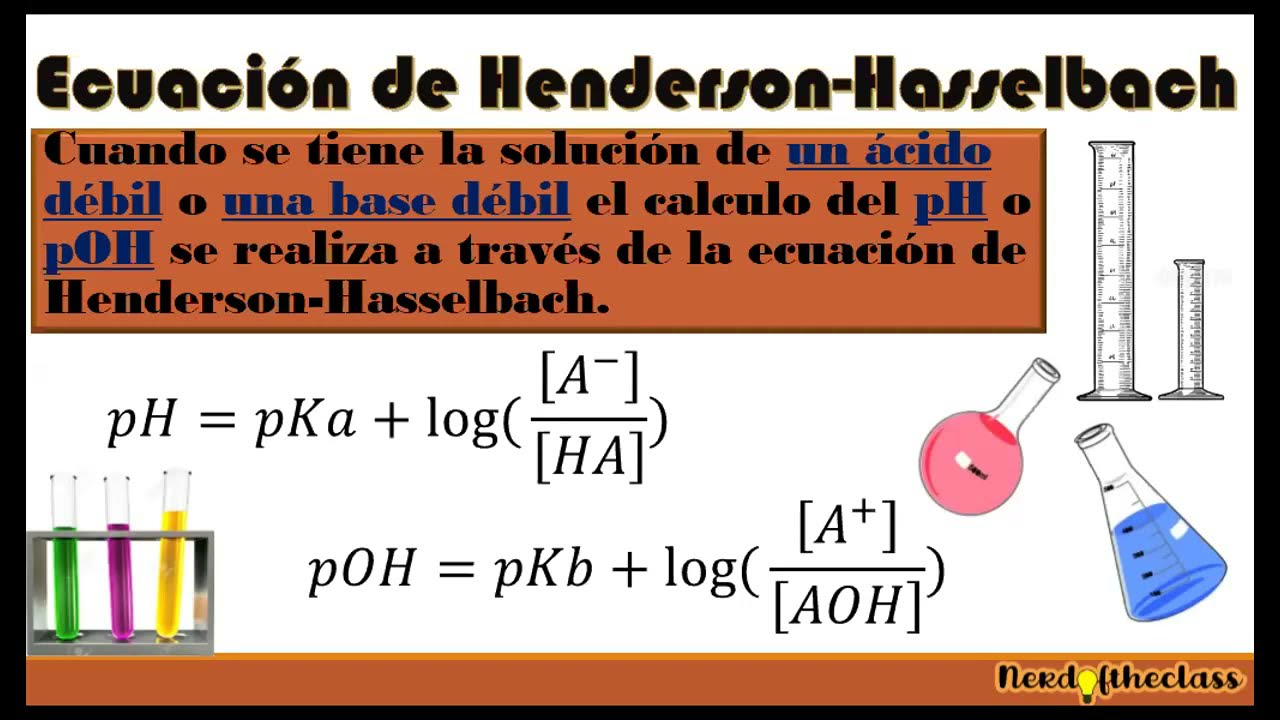
Ecuación de henderson Hasselbach YouTube

(PDF) El uso de la ecuación de HendersonHasselbalch para el cálculo del pH en sangre Dr. Juan

ECUACIÓN DE HENDERSON HASSELBACH DEDUCCIÓN QUÍMICA ANALÍTICA YouTube

Aplicación de la ecuación de HendersonHasselbach VALDEZ MONDRAGÓN DAVID 6FM Los

Ejercicios usando la ecuación de HendersonHasselbalch YouTube

Ecuación de HENDERSONHASSELBACH ¿Por qué el pH de la sangre es 7.35 7.45? YouTube

PPT The HendersonHasselbalch Equation PowerPoint Presentation, free download ID4499608

Como calcular el ph con la ecuación de henderson hasselbach YouTube
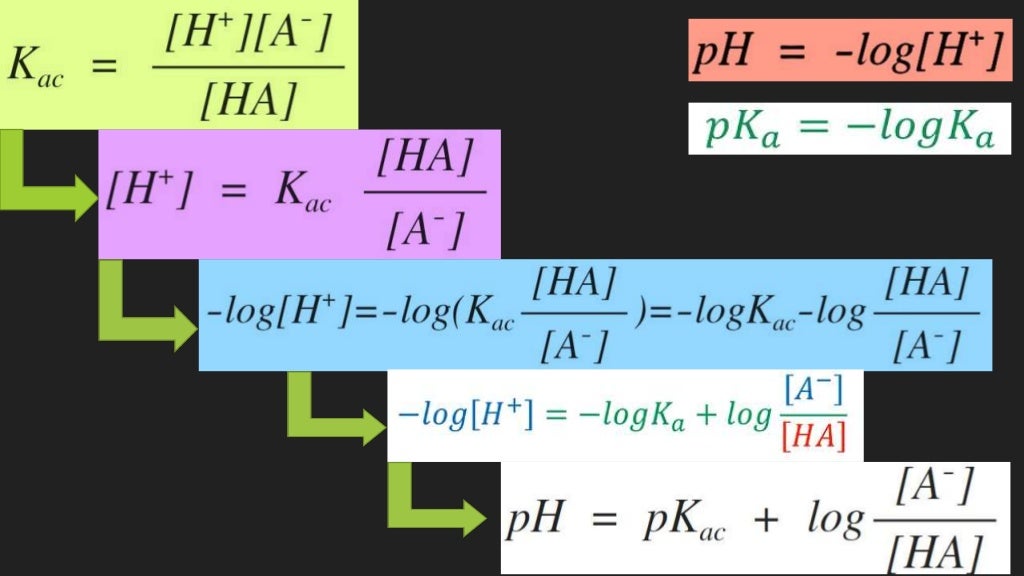
Ecuación de henderson hasselbalch

pH Definición, ácidobase y ecuación de HendersonHasselbalch YouTube
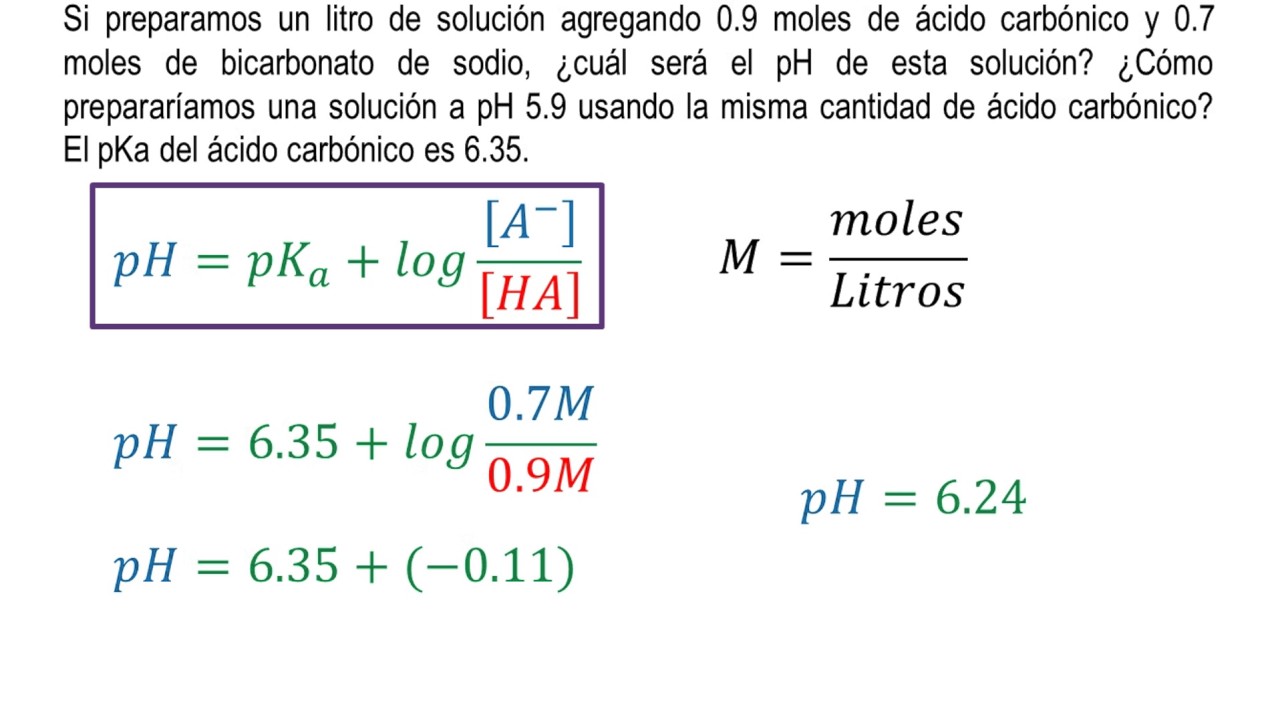
Ecuación de HendersonHasselbalch Ejemplo 1 YouTube
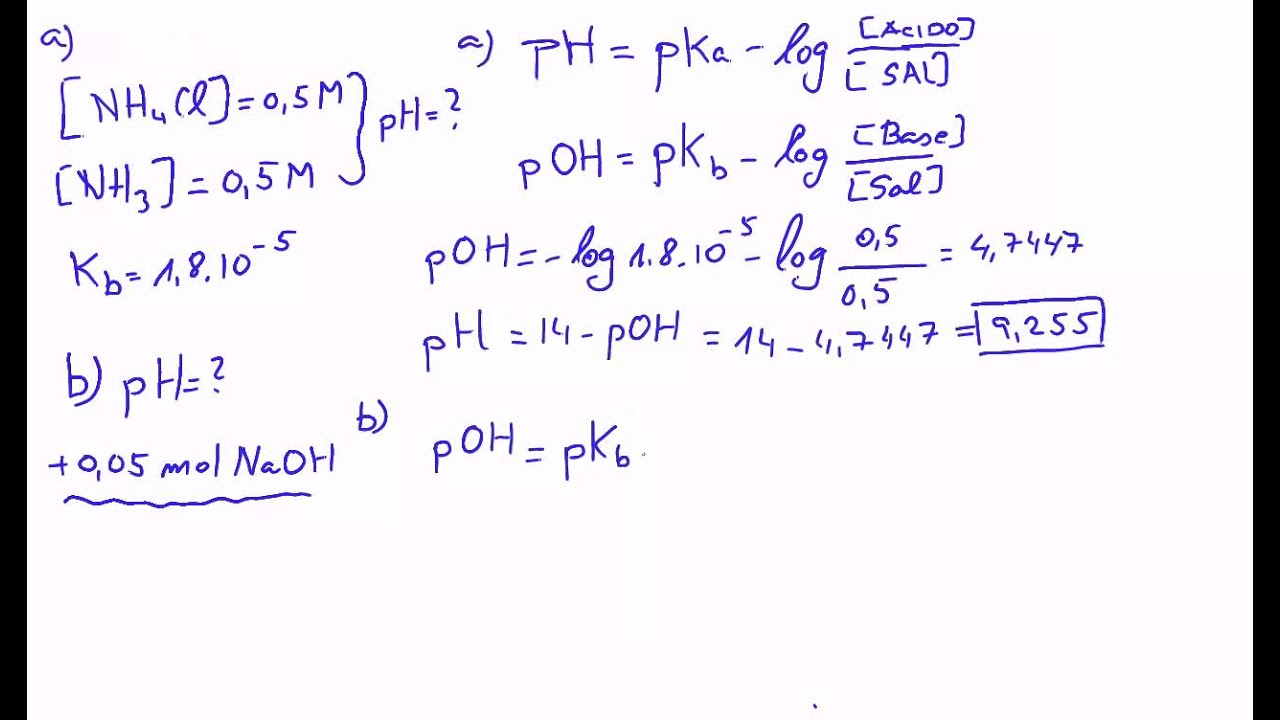
Ecuación de HendersonHaseselbalch YouTube

Ejercicios empleo de la ecuación de HendersonHasselbalch YouTube

PPT FISIOLOGÍA RENAL (Concentración de la orina, Equilibrio AcidoBásico) PowerPoint
3.27. Esta expresión que es la ecuación de Henderson – Hasselbach, permite predecir el grado de disociación que tiene un ácido débil, dependiendo del pH de la solución en la que se encuentre disuelta. La Ecuación 3.27, puede contemplar tres casos:. La ecuación de Henderson-Hasselbalch señala que esta solución está formada por un ácido débil y una base conjugada fuerte expresada como sal. Esta composición le permite a la solución amortiguadora permanecer con un pH estable aunque se le añadan ácidos o bases fuertes. Al añadirle al amortiguador un ácido fuerte, este reacciona con.